4月21日,北京大學(xué)博士后韓益明、北京農(nóng)學(xué)院副教授劉曉曄、安徽農(nóng)業(yè)大學(xué)教授曲少奇作為共同第一作者在Cell雜志在線發(fā)表題為“Tissue geometry spatiotemporally drives bacterial infections”的論文,研究團(tuán)隊(duì)基于多學(xué)科交叉的創(chuàng)新設(shè)計(jì)揭示了宿主組織幾何特性影響細(xì)菌感染的新模式。該研究發(fā)現(xiàn)細(xì)菌在上皮組織中的分布并非傳統(tǒng)認(rèn)為的隨機(jī)模式,而是呈現(xiàn)出明顯的“邊際效應(yīng)”,即細(xì)菌傾向于感染組織細(xì)胞單層邊緣牽引力大的區(qū)域。在此過程中,力敏感的離子通道蛋白Piezo1在介導(dǎo)細(xì)菌感染模式形成的過程中發(fā)揮了重要調(diào)控作用。該研究揭示了“組織細(xì)胞單層幾何結(jié)構(gòu)特性-力信號(hào)轉(zhuǎn)導(dǎo)-感染識(shí)別”主導(dǎo)的病原菌-宿主互作新模式,為開發(fā)針對(duì)多重耐藥菌的宿主導(dǎo)向抗菌療法提供了新的思路和策略。中國(guó)科學(xué)院深圳先進(jìn)技術(shù)研究院研究員黃術(shù)強(qiáng)研究員,北京大學(xué)黃建永研究員,中國(guó)農(nóng)業(yè)大學(xué)朱奎教授為論文的共同通訊作者。

我校青年教師劉曉曄從2018年9月起參與到該項(xiàng)研究中,其中揭示細(xì)胞外基質(zhì)剛度調(diào)控細(xì)菌感染的一部分成果已于2021年在Biomaterials發(fā)表文章。在此項(xiàng)研究中,劉曉曄與合作者從生物學(xué)-力學(xué)融合的角度揭示了組織細(xì)胞幾何特性如何調(diào)控細(xì)菌時(shí)空感染的分子機(jī)制,劉曉曄主要承擔(dān)了Piezo1介導(dǎo)的力學(xué)生物學(xué)信號(hào)轉(zhuǎn)導(dǎo)的分子機(jī)制探索相關(guān)實(shí)驗(yàn),全程跟進(jìn)并主要參與文章的撰寫與修訂。
打破傳統(tǒng)認(rèn)知:宿主組織幾何特性驅(qū)動(dòng)細(xì)菌感染“邊際效應(yīng)”的形成
關(guān)于細(xì)菌和宿主細(xì)胞相互作用的研究通常在非限制的上皮單層內(nèi)進(jìn)行,且細(xì)菌在上皮單層上的分布模式默認(rèn)為是隨機(jī)的。該研究打破了傳統(tǒng)認(rèn)為細(xì)菌感染是隨機(jī)分布的觀點(diǎn),表明宿主細(xì)胞單層的結(jié)構(gòu)特性對(duì)細(xì)菌感染的空間分布具有重要調(diào)控作用。研究者們基于微納加工技術(shù)構(gòu)建了具有不同幾何結(jié)構(gòu)的上皮單層模型,觀察到多種病原菌均在感染初期呈現(xiàn)出邊緣分布模式,即呈現(xiàn)出細(xì)菌感染的“邊際效應(yīng)”(圖1)。該感染模式不受細(xì)胞類型、細(xì)胞單層尺寸和基底修飾方法等因素的調(diào)控,而是與組織細(xì)胞單層的致密度相關(guān),即細(xì)菌感染主要發(fā)生在致密細(xì)胞單層的邊緣。
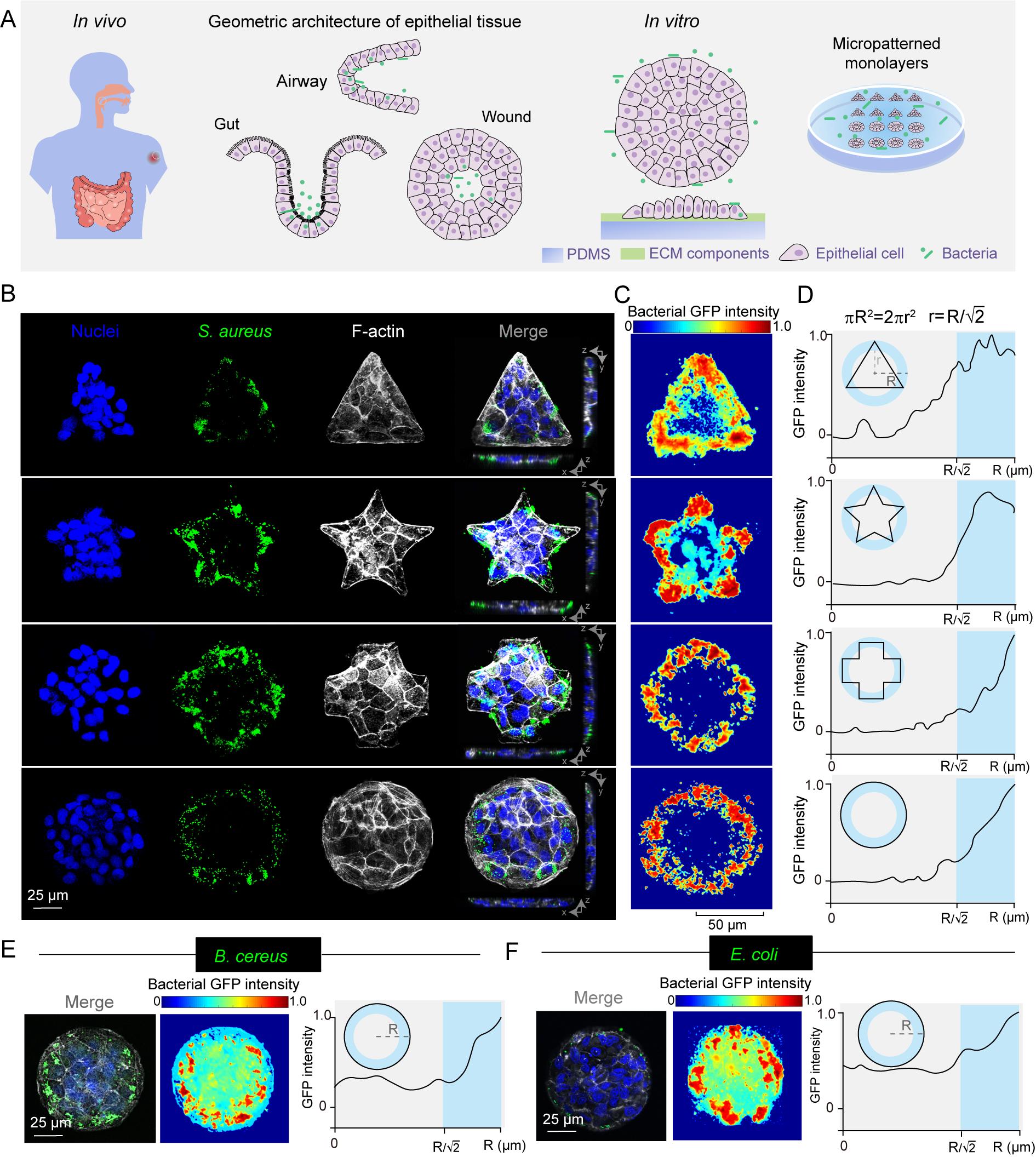
圖1:細(xì)菌感染多細(xì)胞單層呈現(xiàn)的“邊際效應(yīng)”
生物學(xué)-力學(xué)融合:宿主組織細(xì)胞幾何結(jié)構(gòu)邊際的“生物力-感染”效應(yīng)
為了解析細(xì)菌與宿主細(xì)胞單層互作及感染的時(shí)空分布規(guī)律,研究團(tuán)隊(duì)構(gòu)建了上皮細(xì)胞單層與細(xì)胞外基質(zhì)微環(huán)境相互作用的生物力學(xué)模型,揭示了具有幾何約束的上皮單層內(nèi)細(xì)胞牽引力與細(xì)菌感染具有高度協(xié)同性,即細(xì)菌更傾向于感染具有高牽引力區(qū)域的細(xì)胞,這一發(fā)現(xiàn)為理解細(xì)菌感染的空間選擇性提供了新的視角。在此基礎(chǔ)上,研究團(tuán)隊(duì)揭示了力敏感的離子通道蛋白Piezo1在細(xì)菌與上皮細(xì)胞單層互作過程中的關(guān)鍵調(diào)控作用。具體而言,在細(xì)菌入侵宿主細(xì)胞的過程中,Piezo1組裝成囊泡狀結(jié)構(gòu),并在細(xì)菌入侵部位聚集,進(jìn)而促進(jìn)細(xì)菌感染“邊際效應(yīng)”的形成。上述工作不僅揭示了力學(xué)生物學(xué)因素在細(xì)菌感染過程中的關(guān)鍵調(diào)控作用,也為從生物物理力學(xué)視角開發(fā)宿主導(dǎo)向型抗感染療法提供了全新的思路和策略。
力學(xué)生物學(xué)轉(zhuǎn)導(dǎo)機(jī)制:Piezo1蛋白介導(dǎo)細(xì)菌感染模式的形成
Piezo1作為經(jīng)典的力敏感離子通道蛋白,可通過感知和響應(yīng)細(xì)胞外的力學(xué)刺激,激發(fā)細(xì)胞內(nèi)的力信號(hào)轉(zhuǎn)導(dǎo)通路,從而調(diào)控細(xì)胞的生理功能和行為。研究團(tuán)隊(duì)發(fā)現(xiàn),在非感染和感染的幾何限制細(xì)胞單層中,Piezo1的空間異質(zhì)性分布均受到細(xì)胞牽引力的調(diào)控作用。在細(xì)菌感染宿主組織細(xì)胞過程中,研究團(tuán)隊(duì)進(jìn)一步揭示了Piezo1在高牽引力區(qū)域被有效富集和激活,并與入侵細(xì)菌發(fā)生明顯的共定位,隨后,通過Ca2+ 內(nèi)流信號(hào)促進(jìn)細(xì)菌入侵部位p-MLC的組裝,從而加速細(xì)菌在該區(qū)域的感染,形成具有邊際效應(yīng)的感染模式(圖2)。
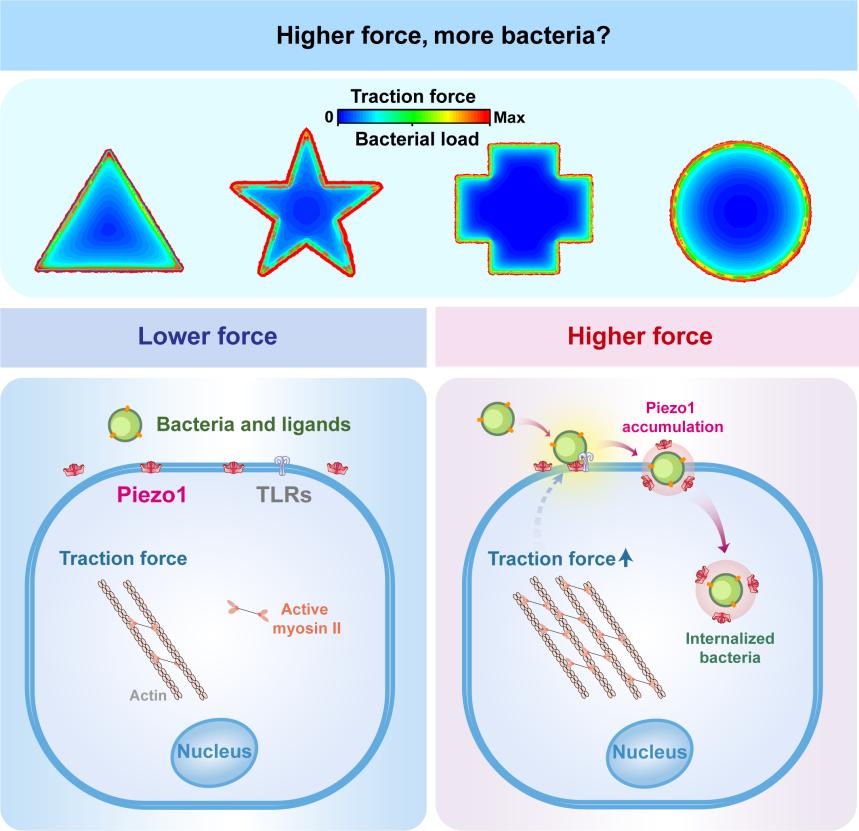
圖2:宿主細(xì)胞單層結(jié)構(gòu)調(diào)控細(xì)菌感染示意圖
器官特性指導(dǎo)精準(zhǔn)給藥:基于宿主導(dǎo)向的新型抗菌策略研究
基于力敏感離子通道蛋白Piezo1在介導(dǎo)多細(xì)胞上皮單層內(nèi)產(chǎn)生的細(xì)胞牽引力調(diào)控細(xì)菌感染過程中的關(guān)鍵作用,研究團(tuán)隊(duì)嘗試將Piezo1作為抗菌靶點(diǎn),并發(fā)現(xiàn)抑制Piezo1的表達(dá)和激活均能明顯降低感染組織中的細(xì)菌載量。進(jìn)一步,研究團(tuán)隊(duì)通過建立仿生3D腸道芯片,成功模擬了具有隱窩等關(guān)鍵形態(tài)特征的宿主腸道細(xì)胞結(jié)構(gòu),觀察到消化道細(xì)菌傾向于在隱窩結(jié)構(gòu)中富集,并發(fā)現(xiàn)這一分布模式與Piezo1的激活密切相關(guān)。基于這一發(fā)現(xiàn),團(tuán)隊(duì)開發(fā)了靶向隱窩結(jié)構(gòu)的“核-殼”藥物遞送系統(tǒng)。通過模擬細(xì)菌的分布規(guī)律,該藥物遞送系統(tǒng)不僅能夠在物理空間上精準(zhǔn)靶向感染位點(diǎn),還能提升抗菌藥物在隱窩結(jié)構(gòu)的局部濃度,提高對(duì)MRSA和VRE感染的療效,為抗菌藥物提質(zhì)增效、降低毒副作用和指導(dǎo)合理用藥提供了潛在方案。
“感謝博士階段的合作導(dǎo)師朱奎教授、博士后導(dǎo)師黃建永教授以及深圳先進(jìn)研究院的黃術(shù)強(qiáng)研究員對(duì)論文的大力指導(dǎo)。”劉曉曄說,“此次合作讓我深刻感受到跨學(xué)科交叉融合的魅力,讓我明白在科研的迷宮中,跨學(xué)科合作就像擁有了一盞明燈,它雖然不能直接給出答案,但總能照亮意想不到的路徑。”

“作為青年教師,我切實(shí)感受到近年來學(xué)校黨委對(duì)青年教師成長(zhǎng)發(fā)展的高度重視和全方位支持。”劉曉曄表示,將緊密圍繞“落實(shí)教育強(qiáng)國(guó)建設(shè)綱要,推動(dòng)學(xué)校事業(yè)高質(zhì)量發(fā)展”主題主線,以“實(shí)干創(chuàng)先年”為抓手,繼續(xù)與中國(guó)農(nóng)業(yè)大學(xué)、北京大學(xué)等高校科研工作者開展跨校、跨方向、跨專業(yè)合作,持續(xù)開展宿主導(dǎo)向的抗菌策略研究,不斷產(chǎn)出高水平科研成果,為耐藥菌防控、人類和動(dòng)物健康保駕護(hù)航。大力弘揚(yáng)教育家精神,著力培養(yǎng)社會(huì)責(zé)任感強(qiáng)、專業(yè)知識(shí)扎實(shí)、富有創(chuàng)新創(chuàng)業(yè)精神和實(shí)踐能力的知農(nóng)愛農(nóng)新型人才,為學(xué)校事業(yè)高質(zhì)量發(fā)展作出積極貢獻(xiàn)。

 最新動(dòng)態(tài)
最新動(dòng)態(tài)


 當(dāng)前位置:
當(dāng)前位置: